

薬事法の改正に伴い2014年11月に施行された医薬品医療機器等法(正式名称:医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律)では、MRI等で撮影された画像データの処理、保存、表示等を行うプログラムのような単体プログラムも、欧米と同様に「医療機器」として製造販売の承認・認証等の対象とすることとなった。現在、「医療機器」に該当するソフトウェアの考え方を取りまとめた政省令類公布のための作業が進行中であり、その詳細は公布されてから追記することにするが、この変更に伴い、実際の規制に引用されうる医療機器ソフトウェア関連国際規格の重要性が増すこととなった。そこで、ソフトウェアに関連した国際標準化の現状を調査し、その現状を関係者に発信することを目的として本ページを開設した。
2016年3月時点の医療機器ソフトウェアを取り巻く国際規格の状況は以下のようになっている。現在も大枠に変化はないと思われていたが、各々の標準の内容は更新されているのみならず、急速に状況は変化していると思われる。ある程度フォローした後、下の概念図は修正することでご容赦いただきたい。
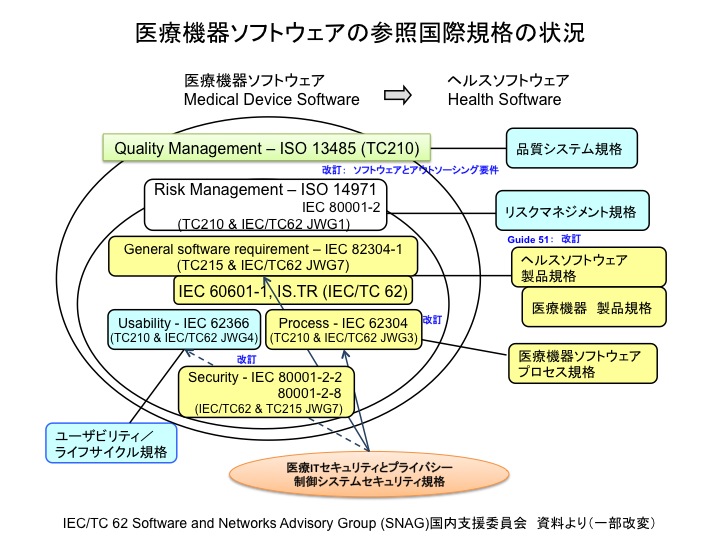
現在作成されている国際標準の傾向として、従来、医療機器に相当するソフトウェアのみを対象とした規格作成が中心だったが、その対象が“Healthcare”と広がってきている。すなわち、一般ユーザも使用するような「医療機器」ではないソフトウェアも含んだ形で規格が作成されるようになってきている(モバイルアプリなど)。よって、規制で明確に医療機器と非医療機器との線引きを行うだけでなく、規格をどのように適用させるかも大きな問題となってきている。国内では、2016年3月31日に「医療機器プログラムの承認申請に関するガイダンス」が発行され、その方向性が示された。また、2015年4月28日に医療機器におけるサイバーセキュリティの確保に関する通知が発出されるとともに、2016年7月にはIoTガイドラインが総務省、経産省、IoT推進コンソーシアムにより公表、医療機器におけるサイバーセキュリティの確保に関するガイダンスが厚生労働省により作成中であり、インターネット接続医療機器のサイバーセキュリティ確保のための環境も整ってきているが、米国と比較すると不十分な面が多いようである。既にガイダンスは発出されているが、その内容は世界状況に比べ遅れている。IMDRFによるガイダンスが発行されたことに伴い上記国内ガイダンスは当該ガイダンスと整合させる形で2018年に改訂された(薬生機審発0724第1号、薬生安発0724第1号「医療機器のサイバーセキュリティの確保に関するガイダンスについて」)。同年、医療機関に対するサイバーセキュリティ確保に関する通知も発出され(医政総発1029第1号、医政地発1029第3号、医政研発1029第1号「医療機関等におけるサイバーセキュリティ対策の強化について」)、医療機器を取り巻く環境は急速に変化している。また、本邦においてもAIを利用した診断支援装置がこれまでに5製品承認されており、AI利用に係る規制及び標準が必要な状況となっている。
上の図からも明らかなように、医療機器ソフトウェアは「医療機器」となるので、製造時には国際的にはTC 210で作成されている品質規格、ISO
13485を満たすことが要求されることになる。2016年2月、ISO 13485の改訂版が発行されたことに伴い、数々のソフトウェア関連規格が相互に引用される状況になり、今後、関連業界に多大な影響を及ぼしている。2020年現在、ISO
13485の2016年版は定期見直しの結果、維持することが確定したため、親標準であるISO 9001:2015との整合は行われず、そのままの項立てでセクター標準として運用されることに落ち着いた様子である。また、ISO
14971の改定版が2019年に発行された。この改定も他の医療機器関連標準に何らかの形で影響を及ぼしている模様である。一方、医療機器ソフトウェア用のプロセス規格であるIEC
63204がヘルスウェアソフトウェアまでも対象とする形で改定作業が進んでいるが、医療機器の特性を反映させた内容とするよう、討議が進んでおり、既に第3版発行に向けた改訂作業が進んでいる。AIに関連した標準化活動も規制側、開発側の両面から活発化しており、今後、フォローすべき事項は益々増えている。
上記図に記載した関連ISO及びIECのTC等の活動状況についてはリンク先に詳細を記す。討議の展開が速く整理が追いついていないことから、更新が不十分な点についてはご容赦いただきたい。
Last update 2021.03.30
Copyright(C) 医療機器部